PENDAHULUAN
Senyawa hidrokarbon terdiri atas karbon dan hidrokarbon.
Senyawa hidrokarbon yang dapat kita temukan dalam kehidupan sehari-hari salah
satunya adalah alkohol. Alkohol sering dipakai untuk menyebut etanol, yang juga
disebut grain alcohol; dan kadang untuk minuman yang mengandung alkohol. Hal
ini disebabkan karena memang etanol yang digunakan sebagai bahan dasar pada
minuman tersebut, bukan metanol, atau grup alkohol lainnya. Begitu juga dengan
alkohol yang digunakan dalam dunia famasi. Alkohol yang dimaksudkan adalah
etanol.
Alkohol dijumpai di alam secara luas,
baik berupa hasil sintesis ataupun secara alami. Senyawa alkohol atau alkanol
dapat dikatakan sebagai senyawa alkana yang satu atom Hnya diganti dengan gugus
–OH (hidroksil). Alkohol adalah gugus hidroksil yang terikat pada karbon
hibridisasi sp3.
RUMUS
UMUM
Senyawa alkohol memiliki rumus umum R-OH dimana R
merupakan gugus alkil. Untuk
itu, rumus umum golongan senyawa ini juga dapat ditulis :
CnH2n + 2OH
TATA NAMA
Penamaan senyawa alkohol prinsipnya ada 2 , yaitu :
1.
Dengan aturan IUPAC
Penamaan
menggunakan aturan IUPAC yaitu menggunakan nama senyawa alkoholnya dengan
mengganti akhiran “ana” menjadi “anol”.
Contohnya :
CH3 CH3OH
Metana Metanol
2.
Dengan sistem trivial
Yaitu dengan
menyebutkan nama gugus alkilnya terlebih dahulu kemudian diikuti kata alkohol.
Contoh :
C2H5OH
Etil alkohol
Untuk senyawa dengan rumus struktur bercabang aturan
penamaannya adalah sebagai berikut :
1.
Tetapkan rantai utama dengan cara
memilih deretan atom C terpanjang yang mengikat gugus OH, kemudian diberi nama
sesuai nama alkohonya.
2.
Pemberian nama pada rantai utama
dimulai dari ujung yang memberikan nomor terkecil bagi atom C yang mengikat
gugus OH.
KLASIFIKASI
Berdasarkan
perbedaan letak terikatnya gugus –OH pada atom C. Alkohol dibedakan
menjadi tiga yaitu :
1.
Alkohol primer yaitu jika
gugus –OH terikat pada atom C primer (atom C yang mengikat 1
atom C yang lain secara langsung )
Contoh
:
CH3 – CH2 –
CH2 – CH2 – OH
n-butanol
2.
Alkohol sekunder yaitu jika gugus –OH terikat
pada atom C sekunder (atom C yang mengikat secara langsung dua atom C yang lain).
Contoh :
3.
Alkohol tersier yaitu
jika gugus –OH terikat pada atom C tersier (atom C yang mengikat
secara langsung tiga buah atom C yang langsung)
Contoh
:
Berdasarkan jumlah gugus fungsinya alkohol
dibedakan menjadi alkohol monovalen dan alkohol polivalen.
1.
Alkohol monovalen adalah alkohol yang hanya
mempunyai satu gugus fungsional – OH.
Contoh : CH3 – CH2 – OH
Etanol
CH3 –
CH2 – CH2 – OH
Propanol
2.
lkohol polivalen adalah jenis senawa
alkohol yang mempunyai gugus fungsional lebih dari satu.
Contoh :
1.
Alkohol
mempunyai titik didih tinggi dibandingkan alkana-alkana yang jumlah atom C-nya
sama. Hal ini disebabkan antar molekul alkohol membentuk ikatan hidrogen
2.
Makin
banyak cabang maka titik didihnya akan semakin menurun
3.
Dalam
air, methanol, etanol dan propanol mudah larut, sedangkan mulai butanol hanya
sedikit larut
4.
Berupa cairan encer dan mudah bercampur
dengan air dalam segala perbandingan
5.
Mudah terbakar
6.
Bentuk fasa pada suhu ruang :
·
dengan C 1 s/d 4 berupa gas atau cair
·
dengan C 5 s/d 9 berupa cairan kental
seperti minyak
·
dengan C 10 atau lebih berupa zat padat
SIFAT SIFAT KIMIA ALKOHOL
1.
Gugus OH merupakan gugus yang cukup reaktif sehingga alkohol mudah terlibat
dalam berbagai jenis reaksi. Contohnya : Reaksi dengan logam aktif Natrium dan Kalium akan membentuk alkoksida
dan gas Hidrogen.
2.
Alkohol sederhana mudah terbakar
membentuk gas karbondioksida dan uap air.
3.
Jika dipanaskan dengan asam sulfat
pekat akan mengalamidehidrasi (melepas molekul air) membentuk eter/alkena.
SINTESIS / PEMBUATAN ALKOHOL
Pembuatan alkohol dapat dilakukan melalui berbagai cara yaitu :
1.
Reaksi subtitusi nukleofilik
Substitusi nukleofilik adalah
suatu kelompok dasar reaksi substitusi, dimana sebuah nukleofil yang
"kaya" elektron, secara selektif berikatan dengan atau menyerang
muatan positif dari sebuah gugus kimia atau
atom yang disebutgugus lepas (leaving
group). Nukleofilisitas adalah ukuran kemampuan suatu pereaksi yang
menyebabkan terjadinya sutu reaksi subtitusi.
Contohnya :
suatu alkil halida alkohol primer
2.
Reaksi Grignard
Reaksi Grignard ditemukan oleh kimiawan Perancis Auguste Victor
Grignard (1871-1935) di tahun 1901. Suatu reaksi grignard yaitu :
a.
Dengan
formaldehid menghasilkan suatu alkohol primer
b.
Dengan aldehid lain menghasilkan suatu
alkohol sekunder.
c.
Dengan keton menghasilkan suatu alkohol
tersier. ]
3.
Reduksi senyawa karbonil
Alkohol dapat dibuat dari senyawa
karbonil dengan reaksi reduksi, dimana atom hidrogen ditambahkan pada gugus
karbonilnya.
Contoh :
Bila suatu alkena diolah dengan air dan
suatu asam kuat, yang berperan sebagai katalis, unsur unsur air mengadisi
(ditambahkan ke dalam) ikatan rangkap dalam suatu reaksi hidrasi. Produknya
adalah alkohol.
Contoh :
5. Etanol dari peragian
Etanol yang
digunakan dalam minuman diperoleh dari peragian karbohidrat yang berkataliskan
enzim (fermentasi gula dan pati ). Satu tipe enzim mengubah karbohidrat ke
glukosa kemudian ke etanol.
enzime
glukosa etanol
Sumber karbohidrat untuk peragian bergantung pada
ketersediaannya dan pada tujuan penggunaan alkohol. Di Amerika Serikat
contohnya, karbohidrat diperoleh terutama dari jagung dan residu molase dari
pabrik gula. Atau dapat juga dari kentang, beras, ubikayu, atau buah buahan (
buah anggur,berri hitam dan sebagainya ).
Peragian buah buahan,sayuran atau biji- bijian berhenti
bila kadar alkohol telah mencapai 14 – 16 %.
KEGUNAAN ALKOHOL
Metanol
·
Bahan membuat pernis
·
Sebagai pelarut
·
Industri zat warna
·
Bahan untuk membuat
metanal
·
Sebagai bahan tambahan pada bensin
Etanol
·
Dalam laboratorium sebagai pelarut
·
Untuk membuat senyawa organik
·
Membuat karet sintesis
·
Sebagai bahan bakar
·
Bahan untuk membuat cuka, kloroform,
iodoform, serta campuran minuman keras.
Propanol/ Propil alkohol
·
Beracun dibandingkan dengan
etanol,digunakan sebagai pelarut.
Butanol
·
Pelarut penting untuk lak nitoselulosa
Pentanol/ Amil alkohol
·
Sebagai pelarut
·
Bahan pembuat amil asetat




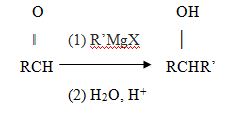



0 komentar:
Posting Komentar